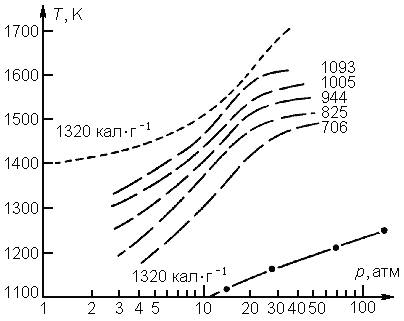
Рис. 27. Характерные зоны при горении двухосновного ТРТ
Характер горения ТРТ зависит главным образом от свойств его компонентов, микроструктуры и режимных параметров. Необходимо делать различие между горением гомогенных [110] и смесевых твердых топлив [23, 143]. Сначала рассмотрим стационарное горение гомогенных ТРТ, а затем приведем обзор различных моделей горения смесевых топлив. При этом особое внимание уделим статистическим моделям, которые могут быть распространены и на нитраминные топлива. Далее выведем основные уравнения для анализа горения СТТ.
При описании механизма горения СТТ сначала рассмотрим горение двух его главных компонентов - ПХА и органического связующего, а затем приступим к рассмотрению моделей горения самого топлива.

В зоне прогрева толщиной порядка нескольких десятков мкм (рис. 27) компоненты гомогенного топлива (нитроглицерин, нитроцеллюлоза, пластификатор, добавки для модификации баллистических характеристик) не реагируют и достигают подповерхностной зоны разложения, известной также под названием пенной зоны. Температура в этой зоне (рис. 28) уже достаточна для того, чтобы инициировать реакции разложения. Здесь происходят разрыв связи СО-NO2 и рекомбинация, так что с поверхности выделяется смесь NO2, альдегидов и NO. Общий энергетический баланс в зоне разложения экзотермический. При давлениях ниже 10 МПа можно различать зоны первичного (зона газификации) и вторичного (светящегося) пламени, которые разделены темной зоной (рис. 27). В первой зоне протекают реакции NO2 с альдегидами, а во второй - реакции NO+CO и NO+NH2. При указанных давлениях вторичное пламя расположено слишком далеко, чтобы оказывать влияние на процессы вблизи поверхности ТРТ, и даже не индуцирует температурный градиент в зоне первичного пламени. В результате на скорость горения влияют лишь процессы в зоне газификации. Такая ситуация соответствует, как правило, закону горения с показателем степени 0,7. С повышением давления вторичное пламя начинает влиять на процессы в зоне газификации, и в дальнейшем обе зоны сливаются. При этом наблюдается переход к закону горения с показателем степени, близким к 1. Температура в зоне вторичного пламени достигает значений 2100-2400 К в зависимости от теплоты сгорания ТРТ.
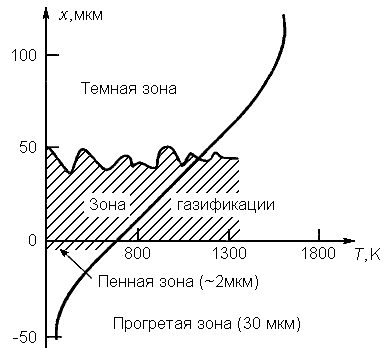
Как следует из рис. 28 и 29, толщина зоны горения чрезвычайно мала, так что детальные исследования здесь весьма затруднены. Для этих целей используются очень тонкие термопары (размером в несколько мкм). Времена пребывания вещества в зоне горения имеют порядок миллисекунды в конденсированной фазе и десятков микросекунд в газовой фазе.
|
Запишем закон сохранения энергии в конденсированной фазе в системе координат, связанной с поверхностью горения (при положительном направлении оси х в сторону газовой фазы) в предположении, что теплофизические свойства за пределами пенной зоны постоянны:
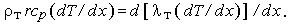 | (3.1) |
Тогда распределение температуры в зоне прогрева имеет вид
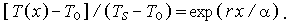 | (3.2) |
Толщина зоны прогрева определяется соотношениями
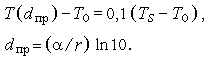 | (3.3a) (3.3б) |
Толщину пенной зоны можно определить по температуре, при которой скорость реакции разложения снижается на порядок по сравнению с ее скоростью на поверхности. Тогда для уменьшения температуры 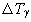 получим
получим
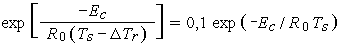 | (3.4) |
при
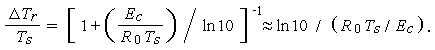 |
Подставляя эту разность температур в (3.2), придем к следующей приближенной оценке толщины зоны разложения:
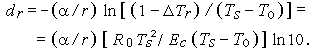 | (3.5) |
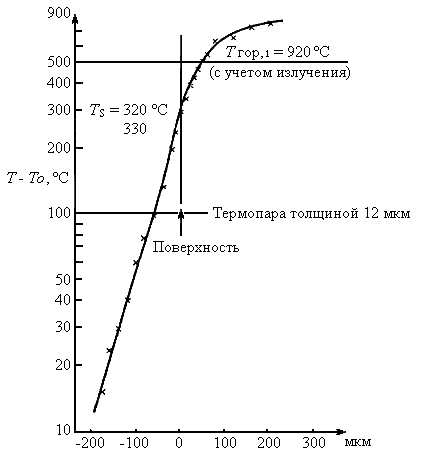
На рис. 30 приведены результаты измерений температурного профиля в образце горящего твердого топлива, полученные с помощью тонких термопар. В работах [98, 184, 185] выполнено множество таких экспериментов с использованием термопар размером в несколько мкм. Распределение температуры, даваемое соотношением (3.2), достаточно хорошо соответствует результатам измерений. Из наклона кривой на рис. 30 получается значение 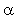 , что согласуется с прямыми измерениями при низких температурах. В работах разных авторов [108, 109, 127, 128, 165] установлено, что значение Еc близко к
, что согласуется с прямыми измерениями при низких температурах. В работах разных авторов [108, 109, 127, 128, 165] установлено, что значение Еc близко к
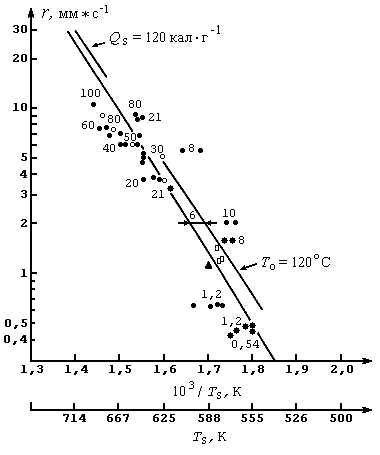
В работе [184] получены данные по суммарной кинетике реакций в зоне горения и установлено, что порядок реакции в зоне первичного пламени равен 1 (по-видимому, инициирование реакции происходит вследствие диссоциации NO2), а энергия активации Eгор,1 равна 5 ккал*моль-1. Порядок реакции в зоне вторичного пламени равен 2, а энергия активации Eгор,2=50ккал*моль-1. Эти результаты показывают, что первичное пламя достаточно толстое, а скорость реакций в ней не очень чувствительна к температуре, тогда как зона вторичного пламени имеет фронтовую структуру с зоной индукции и тонкой зоной активного химического превращения. Зависимость структуры зоны вторичного пламени от давления такова, что при высоких давлениях (более 10 МПа) происходит ее слияние с зоной первичного пламени. Структура пламени в гомогенной среде зависит от распределения температуры и концентраций компонент, которые в свою очередь подчиняются соответствующим уравнениям сохранения.
Для суммарной реакции типа
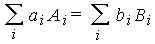 | (3.6) |
имеем
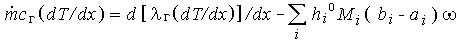 | (3.7) |
и
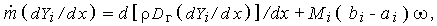 | (3.8) |
где скорость реакции
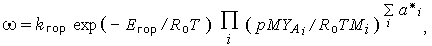 | (3.9) |
причем
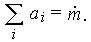 |
Если воспользоваться подобием уравнений, то в предположении близости коэффициентов переноса можно получить следующее соотношение:
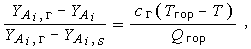 | (3.10) |
где YAt,s - массовая доля компоненты Ai появляющейся вследствие газификации конденсированной фазы.
При больших давлениях, когда зоны первичного и вторичного пламен сливаются, получим в предположении о втором порядке суммарной реакции:
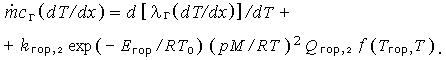 | (3.11) |
В случае реакции с высокой энергией активации в структуре зоны горения можно выделить инертную область с пренебрежимо малой скоростью химического превращения [177]*.
| * Приведенная ниже теория разработана Я. Б. Зельдовичем в 1942г. (см. Я. Б. Зельдович. К теории горения порохов и взрывчатых веществ, ЖЭТФ, 1942, 12 , вып. 11/12, с. 498 - 524). - Прим. перев. |
Профиль температуры в такой области имеет вид
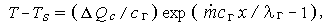 | (3.12) |
где использовано граничное условие на поверхности
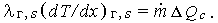 | (3.13) |
Положение фронта пламени над поверхностью определяется из (3.12) при
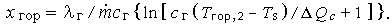 | (3.14) |
Зона горения тонкая, и ее толщина имеет порядок 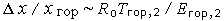 , а падение температуры в ней
, а падение температуры в ней
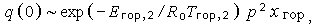 | (3.15) |
и, используя (3.13) и (3.14), окончательно получим соотношение для массовой скорости горения:
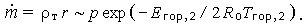 | (3.16) |
Полученный результат характерен для горения при высоком давлении, когда конечная температура пламени постоянна и скорость горения пропорциональна давлению с показателем степени, близким к 1.
При давлении ниже 10 МПа, когда зоны первичного и вторичного пламен отделены друг от друга, можно записать уравнение сохранения энергии для реакции первого порядка:
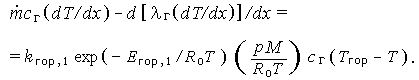 | (3.17) |
При низких значениях Eгор,1 простого решения нет. Чтобы получить некоторое представление, можно задаться приближенным профилем температуры
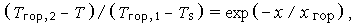 | (3.18) |
который с помощью (3.13) преобразуется к виду
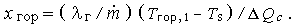 | (3.19) |
Интегрирование (3.17) от поверхности до фронта пламени с учетом (3.18) и (3.19) приводит к выражению
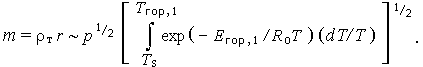 | (3.20) |
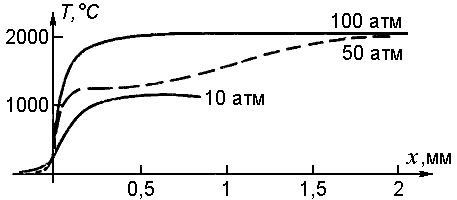
Таким образом, оказывается, что скорость горения пропорциональна давлению в степени 0,5 или больше (если температура Tгор,1 зависит от давления).
Результаты работы [135] свидетельствуют о том, что определяющей реакцией в пламени является реакция NO2 с альдегидом. Исследования этой реакции на плоскопламенной горелке дали значения температуры и скорости распространения пламени, близкие к наблюдаемым при горении ТРТ. Аналогичные результаты получены в ONERA (Франция), причем при подгонке измеренного температурного профиля под соотношение (5.13) подтвердилось, что Eгор,1=5-7 ккал-моль-1. Такой же вывод следует из экспериментов [98]. Результаты измерений температуры в конце зоны первичного пламени [2, 70] показаны на рис. 32. При фиксированном давлении температура Tгор,1 повышается с увеличением теплоты сгорания топлива; с повышением давления температура существенно возрастает.